Лечение мужского бесплодия как социально значимая задача
 В течение последних десятилетий мужское бесплодие приобрело статус серьезной социальной и медицинской проблемы. Патогенез нарушений детородной функции особенно сложный. Разные причины могут привести к неспособности к зачатию. Это делает диагностику и разработку эффективно действующих методов лечения достаточно сложной задачей для медицинских работников. Если проведенная терапия дала неудовлетворительный результат, это означает, что указать с абсолютной точностью причину мужского бесплодия не представляется возможным.
В 2000 году ВОЗ предложил основной критерий для определения бесплодной семейной пары: отсутствие зачатия после года регулярных половых сношений без использования средств контрацепции. Статистические данные по бесплодию существенно различаются в разных странах. Обобщенные данные по всему миру показывают, что в течение одного года 10-25% супружеских пар не могут зачать. 15-50% из их числа обращаются за медицинской помощью. В течение двух лет после начала врачебного наблюдения без применения лечебных средств забеременеть удается каждой четвертой паре. За четырехлетний период наблюдения беременность наступает у каждой десятой пары. Зачатие является невозможным для 2-10% семейных пар. Второй ребенок не может родиться у 10-25% пар.
В современном мире возрастает количество случаев бесплодия у мужчин. На это непосредственное влияние оказывает множество факторов: распространенность заболеваний половой сферы, крайне высокая аллергизация, неблагоприятные воздействия внешней среды, неправильное употребление медицинских препаратов, нездоровый образ жизни, распространение вредных привычек, врожденные патологии органов мочеполовой системы. Медицинские работники разделяют эти факторы на две большие группы: главные (распространены повсеместно) и дополнительные (их негативное воздействие может быть как самостоятельным, так и сочетаться с главными).
В течение последних десятилетий мужское бесплодие приобрело статус серьезной социальной и медицинской проблемы. Патогенез нарушений детородной функции особенно сложный. Разные причины могут привести к неспособности к зачатию. Это делает диагностику и разработку эффективно действующих методов лечения достаточно сложной задачей для медицинских работников. Если проведенная терапия дала неудовлетворительный результат, это означает, что указать с абсолютной точностью причину мужского бесплодия не представляется возможным.
В 2000 году ВОЗ предложил основной критерий для определения бесплодной семейной пары: отсутствие зачатия после года регулярных половых сношений без использования средств контрацепции. Статистические данные по бесплодию существенно различаются в разных странах. Обобщенные данные по всему миру показывают, что в течение одного года 10-25% супружеских пар не могут зачать. 15-50% из их числа обращаются за медицинской помощью. В течение двух лет после начала врачебного наблюдения без применения лечебных средств забеременеть удается каждой четвертой паре. За четырехлетний период наблюдения беременность наступает у каждой десятой пары. Зачатие является невозможным для 2-10% семейных пар. Второй ребенок не может родиться у 10-25% пар.
В современном мире возрастает количество случаев бесплодия у мужчин. На это непосредственное влияние оказывает множество факторов: распространенность заболеваний половой сферы, крайне высокая аллергизация, неблагоприятные воздействия внешней среды, неправильное употребление медицинских препаратов, нездоровый образ жизни, распространение вредных привычек, врожденные патологии органов мочеполовой системы. Медицинские работники разделяют эти факторы на две большие группы: главные (распространены повсеместно) и дополнительные (их негативное воздействие может быть как самостоятельным, так и сочетаться с главными).
Выделяют следующие главные причины мужского бесплодия:
- Варикоцеле;
- Заболевания мочеполовой системы инфекционно-воспалительного генезиса;
- Изолированные патологии семенной жидкости;
- Консервативное лечение (химиотерапия, гормональная терапия, облучение, применение транквилизаторов, препаратов от гипертонии, сульфаниламидов, нитрофурановых производных);
- Наличие заболеваний других органов и систем организма (туберкулез, цирроз печени, диабет, почечная недостаточность, эпидемический паротит при осложнении орхитом, хронические заболевания органов дыхания и пр.);
- Некоторые наркотические вещества;
- Патозооспермия неясного генезиса;
- Патологии, имеющие врожденный характер (крипторхизм, гипоспадия, эписпадия);
- Проблемы с эякуляцией и в сексуальной сфере;
- Прошлые оперативные вмешательства (связаны с лечением патологий мочевого пузыря, паховой грыжи, гидроцеле, а также стриктура уретры);
- Факторы, имеющие иммунологический характер;
- Факторы, имеющие эндокринный характер (первичный и вторичный гипогонадизм, гиперпролактинемия, тестостерондефицитные состояния).
Среди дополнительных причин мужского бесплодия встречаются:
- Неправильное питание;
- Курение;
- Употребление спиртных напитков регулярно;
- Физические травмы внешних органов мочеполовой системы;
- Постоянный контакт с определенными органическими и неорганическими соединениями;
- Выраженная эректильная дисфункция;
- Длительная работа в повышенном или пониженном температурном диапазоне;
- Температура тела выше 38 градусов, которая держится длительное время;
- Психологические причины (семейные ссоры).
Мужское генетическое бесплодие
 В процессе сперматогенеза принимает участие огромное количество предполагаемых генов. Из этого следует, что большинство идиопатических нарушений сперматогенеза связано с мутациями в генах-кандидатах или с полиморфизмом. С целью выявить новые маркеры активно проводились исследования. Правда, они не выявили никаких клинически значимых мутаций и полиморфизмов. Исключение составили мутации, связанные с хромосомой Y. Существенный прогресс в данной сфере возможен при применении новых аналитических подходов.
Почти половина случаев мужского бесплодия обусловливается отклоняющимися от нормы показателями эякулята, при этом в плане и качественном, и количественном. Точная причина бесплодия не выявляется более чем у 30% обратившихся мужчин. В этих случаях врачи говорят о генетическом или иммунологическом факторе воздействия.
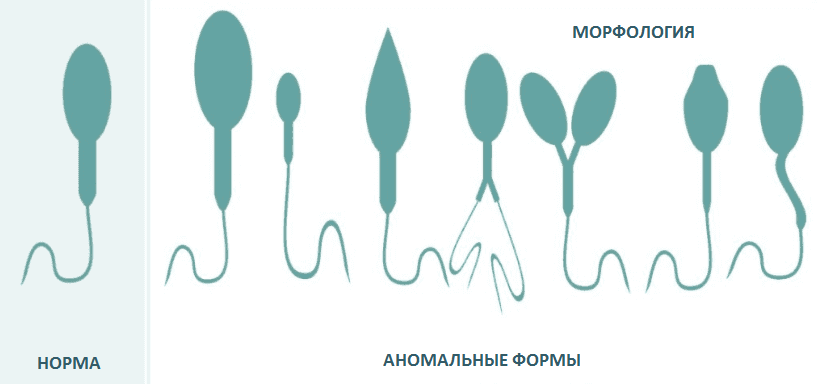
Процесс сперматогенеза очень сложный. Он протекает в несколько этапов. Конечным его результатом становятся зрелые сперматозоиды. При мутации генов, контролирующих этот процесс, происходят морфологические нарушения сперматозоидов, потеря ими подвижности и фертильности. Например, при астенозооспермии в 10-15% случаев обнаруживаются микроделеции хромосомы Y в локусе AZF. Расшифровка анализов спермограммы выявляет изменения этого же участка при тяжелой олигозооспермии (5-10% случаев).
Находящиеся в субрегионе AZFc разные гены объединяются в семейство DAZ (Deleted in Azoospermia). Исследовательские работы сопоставляют неспособность мужчин к зачатию и делеции DAZ2 и DAZ4. Показатели спермограммы пациентов, у которых отсутствуют все четыре гена, значительно хуже, чем у пациентов с сохраненными двумя генами DAZ.
Сильно затрудняет лечение бесплодия у мужчин и целый ряд других генетических факторов. Терапия может быть неэффективна из-за мутаций, которые поразили гены, отвечающие за метаболизм лекарств. Кроме того, определенное воздействие есть и у факторов среды – возникших в результате антропогенного влияния на окружающую среду химических и физических агентов. Они приводят к снижению количественных показателей спермы и уменьшают ее фертильность. Также они могут стать причиной повреждений и мутаций ДНК сперматозоидов, что отрицательно влияет на их двигательную активность и морфологию.
В самом конце XX-го века самый большой интерес приобрела гипотеза, рассматривающая действие эндокринных дизрапторов. Эти вещества способны соединяться с клеточными гормональными рецепторами специфическим образом. Результатом этого является возникновение гормоноподобных эффектов.
Дихлордифенилтрихлорэтан и его метаболиты – одни из самых распространенных эндокринных дизрапторов. Они оказывают непосредственное влияние на производство половых гормонов.
Крайне токсичные вещества дикосины вызывают сильное загрязнение окружающей среды. Их негативное влияние на человеческий организм заключается в замедлении процесса полового созревания, заканчивающегося бесплодием. При этом такому риску подвержены и мужчины, и женщины.
В состав пластмассы входит вещество бисфенол А. Оно очень сильное и может даже в небольшом количестве привести к нарушению сперматогенеза и значительному ускорению полового созревания. В последнее время гиперандрогенность встречается с невероятной частотой. На ее возникновение влияют совершенно разные по происхождению факторы. Принятым объяснением этого факта являются социально-экономические причины, которые можно связать с нарушенным на нейроэндокринном уровне контролем работы желез. Также известен факт, что на экспрессивность проявлений многих генетических болезней влияют самые разные негативные факторы: неблагоприятные воздействия внешней среды, повышенная подверженность инфекциям, ошибки в подборе медикаментозной терапии и др.
В процессе сперматогенеза принимает участие огромное количество предполагаемых генов. Из этого следует, что большинство идиопатических нарушений сперматогенеза связано с мутациями в генах-кандидатах или с полиморфизмом. С целью выявить новые маркеры активно проводились исследования. Правда, они не выявили никаких клинически значимых мутаций и полиморфизмов. Исключение составили мутации, связанные с хромосомой Y. Существенный прогресс в данной сфере возможен при применении новых аналитических подходов.
Почти половина случаев мужского бесплодия обусловливается отклоняющимися от нормы показателями эякулята, при этом в плане и качественном, и количественном. Точная причина бесплодия не выявляется более чем у 30% обратившихся мужчин. В этих случаях врачи говорят о генетическом или иммунологическом факторе воздействия.
Процесс сперматогенеза очень сложный. Он протекает в несколько этапов. Конечным его результатом становятся зрелые сперматозоиды. При мутации генов, контролирующих этот процесс, происходят морфологические нарушения сперматозоидов, потеря ими подвижности и фертильности. Например, при астенозооспермии в 10-15% случаев обнаруживаются микроделеции хромосомы Y в локусе AZF. Расшифровка анализов спермограммы выявляет изменения этого же участка при тяжелой олигозооспермии (5-10% случаев).
Находящиеся в субрегионе AZFc разные гены объединяются в семейство DAZ (Deleted in Azoospermia). Исследовательские работы сопоставляют неспособность мужчин к зачатию и делеции DAZ2 и DAZ4. Показатели спермограммы пациентов, у которых отсутствуют все четыре гена, значительно хуже, чем у пациентов с сохраненными двумя генами DAZ.
Сильно затрудняет лечение бесплодия у мужчин и целый ряд других генетических факторов. Терапия может быть неэффективна из-за мутаций, которые поразили гены, отвечающие за метаболизм лекарств. Кроме того, определенное воздействие есть и у факторов среды – возникших в результате антропогенного влияния на окружающую среду химических и физических агентов. Они приводят к снижению количественных показателей спермы и уменьшают ее фертильность. Также они могут стать причиной повреждений и мутаций ДНК сперматозоидов, что отрицательно влияет на их двигательную активность и морфологию.
В самом конце XX-го века самый большой интерес приобрела гипотеза, рассматривающая действие эндокринных дизрапторов. Эти вещества способны соединяться с клеточными гормональными рецепторами специфическим образом. Результатом этого является возникновение гормоноподобных эффектов.
Дихлордифенилтрихлорэтан и его метаболиты – одни из самых распространенных эндокринных дизрапторов. Они оказывают непосредственное влияние на производство половых гормонов.
Крайне токсичные вещества дикосины вызывают сильное загрязнение окружающей среды. Их негативное влияние на человеческий организм заключается в замедлении процесса полового созревания, заканчивающегося бесплодием. При этом такому риску подвержены и мужчины, и женщины.
В состав пластмассы входит вещество бисфенол А. Оно очень сильное и может даже в небольшом количестве привести к нарушению сперматогенеза и значительному ускорению полового созревания. В последнее время гиперандрогенность встречается с невероятной частотой. На ее возникновение влияют совершенно разные по происхождению факторы. Принятым объяснением этого факта являются социально-экономические причины, которые можно связать с нарушенным на нейроэндокринном уровне контролем работы желез. Также известен факт, что на экспрессивность проявлений многих генетических болезней влияют самые разные негативные факторы: неблагоприятные воздействия внешней среды, повышенная подверженность инфекциям, ошибки в подборе медикаментозной терапии и др.
Под воздействием микросомальной системы метаболизма или системы цитохрома Р-450 реализуются две важнейшие функции:
- эндогенный метаболизм;
- начальная фаза биотрансформации поступающих извне ксенобиотиков, в результате чего формируются функциональные гидрофильные группы.
СТОИМОСТЬ
| Услуга | Цена, руб. |
|---|---|
| Спермограмма с морфологией по критериям Крюгера и МАР тестом | 3300 |
| Комплекс на воспаление (включает секрет предстательной железы - микроскопия) | 2800 |
| Консультация уролога и репродуктолога (при необходимоти с назначением лечения) | 2500 |
Смотрите также